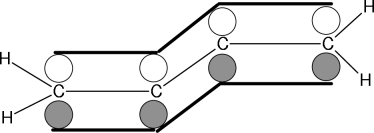
Die beiden Doppelbindungen teilen sich dasselbe
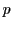
-Orbital. In 1-3-Butadien (als Beispiel) sind die
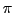
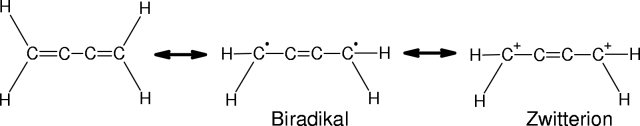
-Bindungen, die die Doppelbindungen ausmachen auf das ganze Molekül verteilt. Es gibt drei mesomere Grenzformeln:
Keine dieser mesomeren Grenzformeln wird jedoch angenommen, sondern das Molekül teilt die
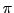
-Bindungen unter allen C-Atomen auf, so daß das Molekül eine niedrigere Energie hat. Molekülsituationen, in denen nicht alle C-Atome die
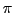
-Bindungen teilen können gezeichnet werden, indem man die
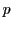
-Oribale der benachbarten C-Atome falsch dreht, so dass nicht mehr der positive Teil des Orbitals den positiven Teil des anderen
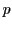
-Orbitales überlappen kann. (Siehe Bindungstheorie):