Cyclobutan
Cyclobutan ist ein Vierer-Ring. Die Winkelspannung des Ringes ist abgeschwächt, da ein weiteres Kohlenstoffatom hinzu gekommen ist. Allerdings gibt es nun Torsionsspannungen wegen der ekliptisch angeordneten Wasserstoffatome, die sich abstoßenden. Somit ist die Gesamtenergie, die bei einer Reaktion frei werden kann, fast gleich geblieben. Allerdings reagiert das Cyclobutan erst nach dem Überwinden einer höheren Barriere. Das theoretische planare Cyclobutan sieht wie folgt aus:
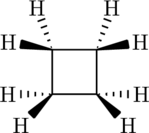
Die Torsionsspannung, verursacht durch die sterische Abstoßung der H-Atome, wird abgeschwächt, indem es zwei rasch aufeinander wechselnde Konformere gibt, bei denen der Ring gefaltet wird. Das Molekül ist nicht planar: