Unterabschnitte
ElektrolyseSchaubildAls Schaubild ist das Daniell-Element, ein galvanisches Element, gezeigt, welches zur Zeit jedoch elektrolysiert, d.h. geladen wird. Eine Elektrolyse zur Gewinnung von Zinn könnte man auch ohne Diaphragma machen. Normalerweise verläuft eine Elektrolyse ohne Diaphragma. Es enstehen an beiden Elektroden Elemente, die häufig gasförmig sind. So entsteht bei der Elektrolyse von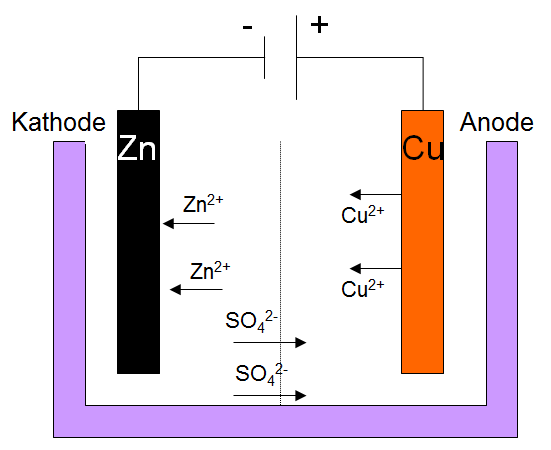
ZersetzungsspannungBei der Elektrolyse scheiden sich nicht sofort Stoffe an den Elektroden ab. Man muß zuerst eine gewisse Spannung überwinden, bevor die Elektrolyse in Gang kommt. Diese Zersetzungsspannung setzt sich zusammen aus der Differenz der Redoxpotenziale und der Überspannung.Dass die Spannung der galvanischen Zelle einer Elektrolyse hinzugeführt werden muß, kommt dadurch zustande, daß zuerst, zum Beispiel bei der Elektrolyse von ÜberspannungZusätzlich zur dieser Spannung kann eine Überspannung existieren. Die Überspannung muß noch einmal hinzuaddiert werden. Die Übergangsspannung ist abhängig von dem Material der Elektroden. An ein und demselben Elektrodenmaterial haben auch unterschiedliche Ionen unterschiedliche Überspannungen. Somit kann man durch eine geschickte Wahl der Elektroden das Redoxpotential zweier Stoffe austauschen, so daß man statt des einen Stoffes bei der Elektrolyse den anderen Stoff gewinnen kann. Dies wird zum Beispiel im Amalgan-Verfahren ausgenutzt, indem Natrium noch vor Wasserstoff an der Quecksilberelektrode abgeschieden wird.Platinierte Platinelektroden haben keine Überspannung. Deshalb kommt auch in der Normalwasserstoffhalbzelle eine platinierte Platinelektrode zum Einsatz. Abscheiden mehrerer gelöster unterschiedlicher IonenIonen, die ein vom Betrag her höheres Redoxpotential mit Einberechnung der Überspannung haben, werden zuerst abgeschieden. Gibt es keine dieser Ionen mehr, folgen die nächst niedrigeren. |