Darstellung Halogene (7.Hauptgruppe) Unterabschnitte
Darstellung Halogene (7.Hauptgruppe)FluorElektrolyse vonFluor wird an der Anode oxidiert, Wasserstoff an der Kathode reduziert. ChlorMit dem Weldon-Verfahren im Labor:Mit dem Amalgan-Verfahren: Das Verfahren hat zwei getrennte Zellen. In der einen Zelle wird NaCl-Lösung mit einer Quecksilberelektrode und beispielsweise einer Kohleelektrode elektlysiert. Die Quecksilberelektrode vertauscht die Potentialhöhe von Wasserstoff und Natrium, so daß die Quecksilberelektrone zu einer Amalgamelektrode wird, indem Natrium sich mit ihr vermischt. An der anderen Elektrode tritt Chlor aus. Mit dem Diphragma-und Membran-Verfahren: Es wird NaCl in Wasser elektrolysiert. Es tritt Wasserstoff und Chlor aus. 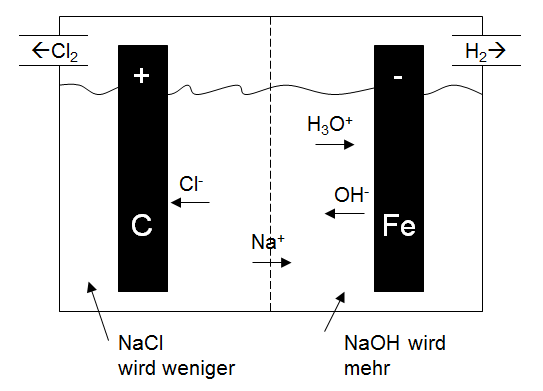
BromLösungen die Brom-Anionen (Alternativ kann Wasserstoffbromid mit Schwefelsäure versetzt werden: |