Konkurrenz zwischen SN2 und SN1
SN2 und SN1 konkurrieren miteinander. Anhand folgender Tabelle läßt sich entscheiden, nach welchem Reaktionsmechanismus die Reaktion abläuft.
| SN2 | SN1 | |
| Substrate | primäre C-Atome (Reaktion findet immer nach S |
tertiäre C-Atome (immer über S |
| Nukleophile | Gute werden bevorzugt. | Kein Einfluss des Nukleophils auf die Reaktion, da zuerst ohne Einfluss des Nukleophils das Substrat auseinander fällt. Deshalb kann man mit einem guten Nukleophil hin zu der Konkurrenzreaktion S |
| Bedingungen | läuft bei niedrigen Temperaturen | hohe Temperaturen besser oder sogar erforderlich, da sich Substrat von Abgangsgruppe trennen muss. |
| Lösungsmittel | Polare aprotische Lösungsmittel zwingen zu S |
Polare protische Lösungsmittel zwingen zu S |
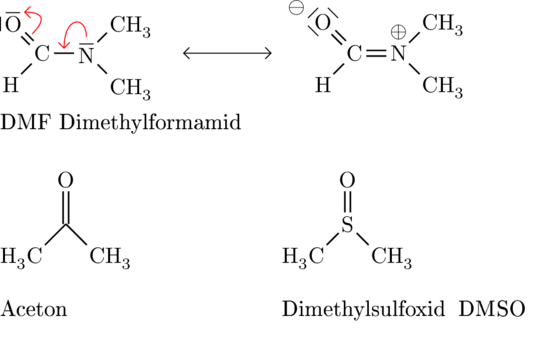
Beispiele für polare aprotische Lösungsmittel: